بعدما وضع الأبحاث العلمية تحت مظلة القانون.. التجارب السريرية نهاية بيزنس المتاجرة بأجساد المرضى
المعهد القومى للكبد قاهر «فيروس سى»
«الأخبار» داخل أول مركز معتمد للبحوث الإكلينيكية فى وزارة الصحة
تجارب «السوفالدى» نجحت بنسبة 99% و«لجنة الأخلاقيات» تراقب الأبحاث الجديدة
قانون البحوث الإكلينيكية.. حماية للمريض والطبيب
يشترط موافقة المريض وعقد تأمين طبى.. والعقوبات تصل للسجن المشدد وغرامة مليون جنيه
تشكيل مجلس يضم الصحة والدفاع والداخلية وأساتذة الجامعات لوضع المعايير والضوابط
«التجارب السريرية» مصطلح ربما يسمعه الشعب المصرى لأول مرة من خلال وسائل الإعلام عقب إصدار مجلس النواب قانون تنظيم البحوث الطبية الإكلينيكية، إلا أن حقيقة الأمر، كشفت أن تلك التجارب كانت تمارس فى الخفاء دون تنظيم أو توفير غطاء لحماية المرضى وهو ما كان يجعل المصريين فئران تجارب للشركات الطبية والدوائية من خلال بيزنس سرى مع بعض الأطباء، إلا أن القانون الجديد وضع ضوابط أخلاقية ومهنية وعقوبات رادعة لتنظيم التجارب السريرية وحماية المريض،وقد تصل العقوبات على المخالفين للسجن المشدد وغرامة مليون جنيه.
تجارب إكلينيكية ناجحة خرجت من مركز أبحاثه، والعديد من الأدوية المهمة التى ساهمت فى إنقاذ حياة المصريين وقهرت أمراضا خطيرة مثل «فيروس سي» تم دراستها داخل معامله وبأيدى أطبائه، ليخرج دواء محلى إلى النور ينافس المنتجات العالمية، أنه المعهد القومى لابحاث الامراض المتوطنه والكبد، الذى قامت «الأخبار» بزيارته وتعد وحدة أبحاثه هى الأولى التى تسجل وتعتمد فى وزارة الصحة وفقاً لشروط صعبة تراعى المعايير الدولية، وخرج من أروقتها تجارب مهمة، أبرزها تجارب أدوية فيروس c مثل السوفالدى وكيوريفو والأوليسيو وغيرها من الأبحاث المهمة فى مجال أمراض الكبد.
استقبلتنا د. سهير شومان رئيس مركز الأبحاث بالمعهد القومى للكبد، وعضو لجنة الاخلاقيات بالمعهد لشرح المراحل التى تمر بها البحوث الطبية الإكلينيكية وحتى خروجها إلى النور، وأكدت أن القانون الجديد هدفة تنظيم عملية البحوث الإكلينيكية فقط وليس لها علاقة بالابحاث الطبية العادية أو رسائل الماجيستر والدكتوراه، وأشارت إلى أن أهم ما يتضمنه القانون الجديد هو حماية المبحوثين وهم المرضى والمواطنون التى يجرى التجارب عليهم، التى بنص القانون يجب أخذ موافقته على البحث وعمل وثيقة تأمين له، كما نص القانون على عدم سفر العينات إلى الخارج إلى عن طريق الجهات المختصة ومن يخالف ذلك توقع عليه عقوبات كبيرة قد تصل إلى الحبس.
وأضافت أن القانون الجديد الزم المراكز البحثية بالعديد من الاشتراطات منها المكان والتجهيزات التى يتم توافرها، دور المريض فى البحث وحمايته والتأمين عليه، والهيكل الطبى والإدارى للمراكز وغيرها من الاشتراطات الحازمة من أجل اعتماد المركز فى وزارة الصحة، وأشارت إلى أن مركز ابحاث معهد الكبد يعد أول مركز يسجل ويعتمد فى وزارة الصحة واجرى فيه العديد من الأبحاث خاصة أدوية فيروس C مثل السوفالدي وكيوريفو والأوليسيو التى تخطت نسبة نتائجها 99% وأجريت على 100 مريض فى المرحلتين الثالثة والرابعة.
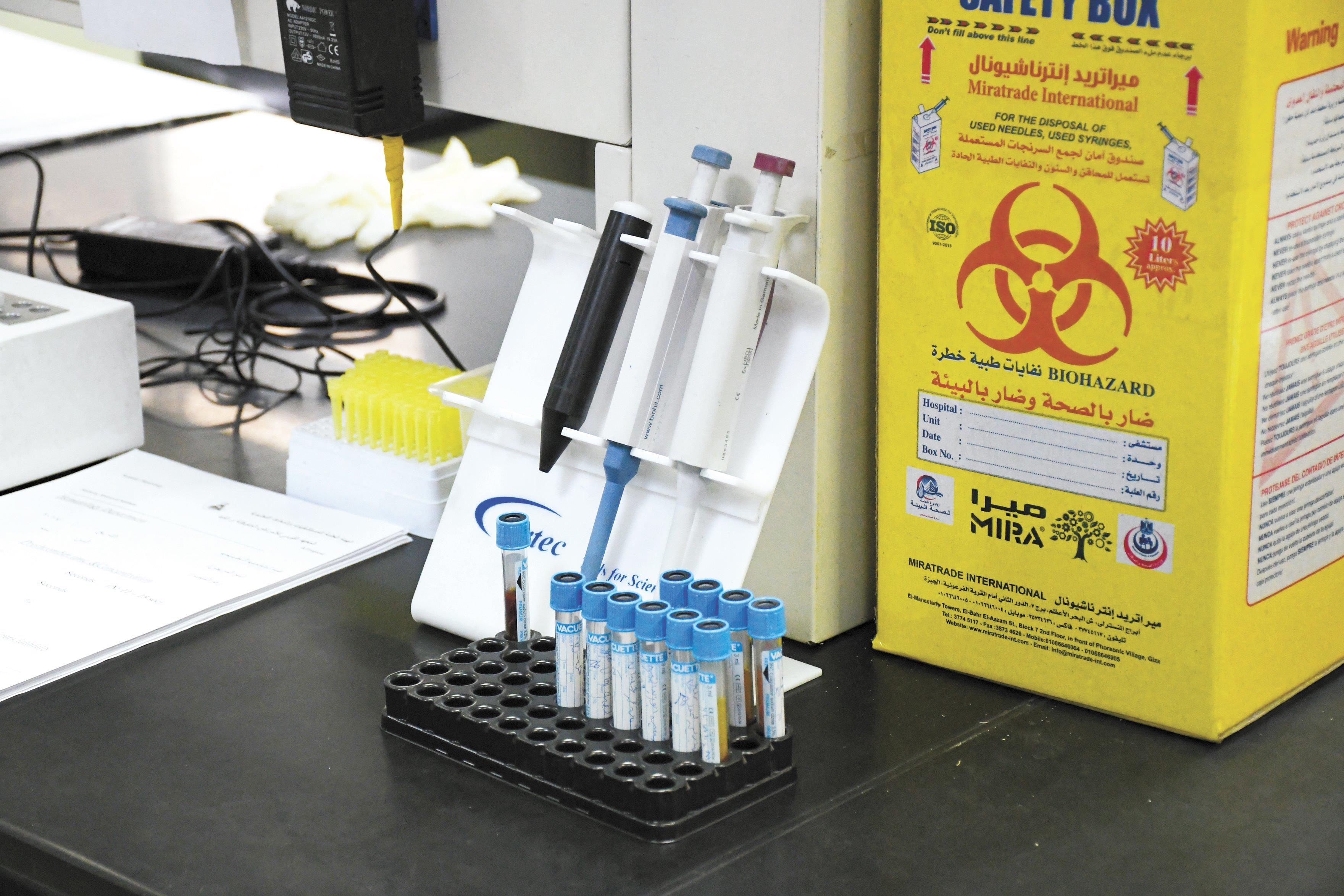
وقامت «الاخبار» بجولة داخل مركز الأبحاث للتعرف بشكل عملى على المراحل التى تمر بها البحوث الإكلينيكية المعروف بـ «التجارب السريرية» وفقاً للاشتراطات التى وضعها القانون، والتى تبدأ من المكتب الإدارى وهو مخصص لرئيس المركز الذى يستقبل فيه الأطباء والباحثين ومندوبى الشركات المحلية والدولية، لتقديم بروتكول البحث الذى تتم دراسته من خلال لجنة أخلاقيات البحث العلمى التى تراجع البحث مهنياً وعلمياً وأخلاقياً،لضمان مراعاة كل الاشتراطات الخاصة بالتجربة والرقابة عليها.
بعد الموافقة على البحث تبدأ المرحلة الثانية داخل قاعة محاضرات مصغرة،نصت عليها الاشتراطات، وذلك من اجل عقد اجتماعات بين الباحثين والأطباء وممثلى الشركات الراعية لشرح كل تفاصيل البحث وطريقة العمل والخطة الموضوعة، ثم تأتى المرحلة التى تليها من خلال غرفة «العيادة» التى يتم فيها مقابلة الأطباء المشاركين فى البحث مع المبحوثين والمرضى الذين وافقوا على اجراء البحث عليهم، ويتم خلال المقابلة شرح كل تفاصيل البحث والاتفاق على مواعيد الزيارات وأخذ العينات وصرف العلاج، كما يتم صرف بدل انتقال فقط لبعض المرض ولا يحصل المريض على أجر مقابل خدمته العلمية ولكن يلزم القانون الباحثين التأمين على المريض واستكمال علاجه حتى بعد انتهاء البحث أو علاج الأعراض الجانبية اذا ظهرت عليه نتيجة للبحث.
وتبدأ بعد ذلك مراحل أخذ العينات من خلال المعامل واجراء البحوث عليها وصرف الأدوية من خلال الصيدلية الموجودة داخل المركز التى تحتوى على ثلاجات لحفظ الأدوية الخاصة بالابحاث، كما يحتوى المركز على أرشيف يضم كل ملفات المرضى إلكترونياً وورقياً «هارد كوبي» تضم كافة بيانات المريض وتطورات علاجه حتى ظهور النتائج.
من جانبه، أكد د. أمين عبد الباقى،رئيس لجنة الأخلاقيات بالمعهد، أن دور اللجنة الرقابة على البحث الطبى المقدم للمركز البحثى، ومتابعة الأبحاث ومعرفة طبيعتها وسؤال المرضى ومعرفة هل اجراءات البحث تتم بصورة صحيحة من عدمه. وأوضح انه لم يتم رصد اى شكاوى اثناء اجراء البحوث فى مركز الابحاث بالمعهد سوى احد المرضى من مدينة طنطا اصيب بأعراض جانبية نتيجة خضوعه لبحث وتمت متابعة ذلك وفحص الشكوى وبعدها اتخذت اللجنة قرارا بإيقاف البحث قانون تنظيم البحوث الطبية الإكلينيكية أو المعروف إعلامياً بـ « التجارب السريرية»،أثار العديد من التساؤلات فى أذهان المواطنين، لذلك تنشر «الأخبار» قراءة فى المواد التى نص عليها قانون البحوث الاكلينكية، متمثلة فى إنشاء مجلس أعلى للبحوث الطبية الاكلينيكية يضم ممثلين من وزارات الصحة والدفاع والداخلية ومن الجامعات والشخصيات العامة، وظيفته وضع معايير وضوابط خاصة بأخلاقيات البحوث الطبية، والتفتيش الدورى على كل الجهات البحثية التى تجرى بها البحوث الطبية فى مصر.
وتضمن القانون انشاء لجنة تسجل فى وزارة الصحة داخل كل منشأة بحثية تسمى «اللجنة المؤسسية لأخلاقيات البحث العلمي»، تختص برعاية حقوق وأمان ومصلحة المبحوثين الذين سيجرى عليهم البحث مع مراقبة الباحث الرئيسى وراعى البحث وهو من يمول البحث العلمى.
وحدد القانون أربع مراحل للأبحاث الطبية الاكلينيكية، الأولى تجرى على عدد من 20 الى 80 مبحوثا، والثانية تجرى على عدد من 200 الى 300 مبحوث، وتهدف المرحلتان للتأكد الكامل من أمان التدخل الطبى، ثم المرحلة الثالثة من البحث على مجموعة من المبوحثين يتراوح عددهم بين المئات والآلاف لمعرفة مدى فاعلية التدخل، أما المرحلة الرابعة وتعرف بمرحلة ما بعد التسويق لتراقب وتضمن الأمان المستمر للدواء بعد حصوله على ترخيص التداول.
واشترط القانون حصول الباحث على موافقة موقعة ومبصومة من المبحوثين تسمى بـ «الموافقة المستنيرة» للبدء فى اجراء البحث مع عدم إجراء أى بحث على الفئات التى لاتستطيع أن تعطى تلك الموافقة مثل الاطفال وذوى الاحتياجات الخاصة، ووضع سقف زمنى يصل الى 120 يوما للحصول على موافقة الدولة لإجراء تلك البحوث. كما وضع القانون عدة شروط لابد من توافرها فى الباحثين اولها أن يكون مستوفيا لكافة المؤهلات العلمية، واذا حدث أى مضاعفات او آثار جانبية على المبحوثين يتم انهاء البحث مباشرة ويمنع هذا الباحث من اجراء أية أبحاث أخرى لمدة عامين.
وألزم القانون راعى البحث الذى سيمول البحث، بالابلاغ الفورى للمبحوثين المشاركين فى البحث الطبى بأية تعديلات تجرى عليه، وبأية نتائج يمكن أن تؤثر بالسلب على سلامتهم وبالآثار الجانبية الخطيرة غير المتوقعة للبحث الطبى، مع الالتزام بإبرام عقد تأمين طبى لهم طيلة البحث الطبى مع اضافة عام آخر فى هذا القانون كإجراء احترازى، فضلاً عن تقديم العلاج اللازم لهم فى حالة الاصابة ذات الصلة بالبحث الطبى واستكمال العلاج لمن يثبت حاجته لذلك منهم حتى بعد انتهاء البحث. ووضع القانون عقوبات رادعة لكل من يخالف نصوص القانون تصل إلى السجن المشدد وغرامة 500 ألف جنيه إذا حدث عاهة مستديمة على المبحوث، والسجن المشدد الذى لا تقل مدته عن 10 سنين وغرامة تصل الى مليون جنيه عند التسبب فى وفاة شخص، والسجن المشدد وغرامة تصل الى مليون جنيه فى حال تهريب أى عينات بشرية أثناء إجراء البحث او بعد الانتهاء منها الى خارج البلاد.